Genomica funzionale per l’immunoterapia
Introduzione
Il sistema immunitario svolge un ruolo fondamentale nel proteggere l'organismo dal cancro, identificando ed eliminando le cellule tumorali. Tuttavia, man mano che i tumori evolvono, accumulano mutazioni e alterazioni cromosomiche che rimodellano la loro capacità di innescare risposte immunitarie—fenomeno noto come immunogenicità tumorale. Mentre alcuni tumori sfruttano questi cambiamenti genomici per evadere il riconoscimento immunitario, altri diventano più immunogenici, aumentando la loro suscettibilità alla sorveglianza immunitaria e all'immunoterapia.
Una domanda centrale che guida la nostra ricerca è: in che modo i meccanismi di riparazione del DNA e l'instabilità genomica influenzano la dinamica interazione tra le cellule tumorali e il sistema immunitario?
Per rispondere a questa domanda, integriamo screening funzionali ad alto rendimento—sia in vitro che in vivo—con approcci avanzati di biologia molecolare e cellulare. Il nostro obiettivo è identificare fattori di risposta al danno al DNA (DDR) e mutazioni puntiformi, in particolare varianti a singolo nucleotide (SNVs), che influenzano l'immunità antitumorale e la risposta all'immunoterapia. In ultima analisi, miriamo a tradurre queste scoperte in strategie innovative di immuno-oncologia che migliorino il riconoscimento immunitario e superino la resistenza dei tumori alla terapia.
Progetti di Ricerca in Corso
1. Identificare i Regolatori dell’Immunogenicità Tumorale
I tumori con difetti nei meccanismi di riparazione del DNA possono attivare risposte immunitarie attraverso la presenza di DNA citosolico, l'aumento del carico mutazionale e la promozione della morte cellulare immunogenica. Tuttavia, i fattori della DDR coinvolti nella regolazione di questi processi rimangono in gran parte non caratterizzati.
Al fine di identificare tali fattori, utilizziamo piattaforme di screening CRISPR-Cas9 sviluppate nel nostro laboratorio, che permettono di quantificare sistematicamente l'impatto dei fattori della DDR e delle loro interazioni genetiche sulla segnalazione immunitaria, identificando così i regolatori chiave dell'immunogenicità tumorale. Mediante questo approccio, ci proponiamo di identificare nuovi bersagli terapeutici in grado di potenziare il riconoscimento immunitario dei tumori.
2. Decifrare l’Impatto delle SNVs sull’Immunogenicità Tumorale
Molte SNVs associate al cancro rimangono poco comprese e sono classificate come varianti di significato incerto. Determinare il loro impatto sulla risposta all'immunoterapia è fondamentale per identificare nuovi biomarcatori e opportunità terapeutiche.
Tramite l'editing di basi dipendente da CRISPR, introduciamo SNVs tumorali su larga scala in geni coinvolti nella risposta al danno al DNA e segnalazione immunitaria, consentendoci di valutarne l'impatto sulla riparazione del DNA e sull'immunogenicità del tumore. Attraverso questo approccio, miriamo a classificare mutazioni responsabili dell'evasione immunitaria e della resistenza alla terapia, aprendo la strada a trattamenti antitumorali più efficaci e personalizzati.
3. Definire il Ruolo della DDR nei Linfociti T CD8+
Il danno al DNA indotto da terapie anti-cancro può compromettere l'attività dei linfociti T CD8+, che tuttavia svolgono un ruolo cruciale nell'immunità antitumorale. Comprendere come queste cellule rispondono allo stress genotossico indotto da tali terapie è essenziale per sviluppare strategie combinatoriali efficaci che le integrino con l'immunoterapia.
Siamo particolarmente interessati a identificare le vie di riparazione del DNA che preservano la funzionalità dei linfociti T in queste condizioni, con l'obiettivo di migliorarne la resilienza e ottimizzare i risultati dell'immunoterapia.
Photogallery
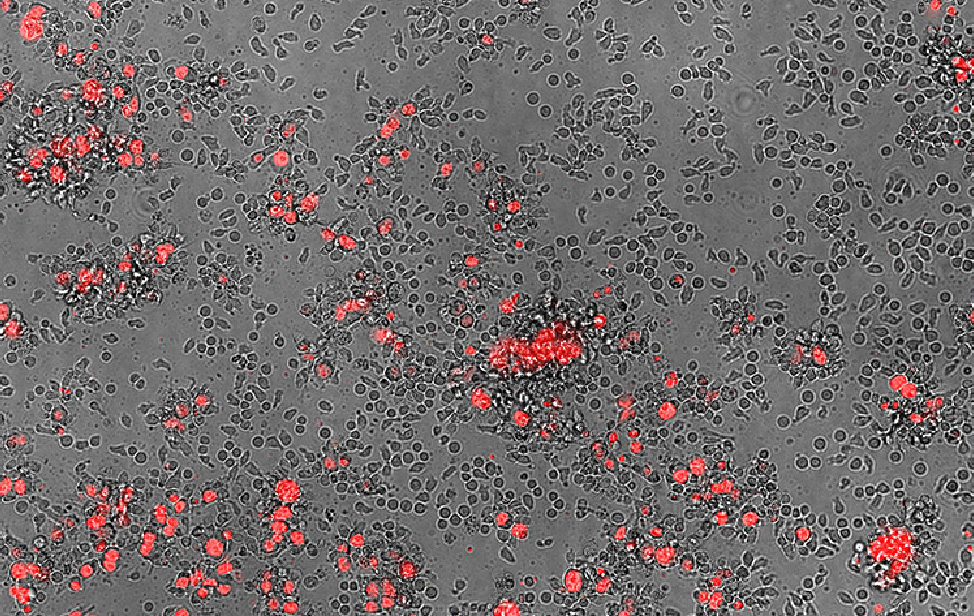 A composite fluorescence and phase contrast microscopy image showing human CD8+ T cells and MDA-MB-436 breast cancer cells (red). The red fluorescence highlights the cancer cells, while the phase contrast reveals the T cells and their interactions with the cancer cells.
A composite fluorescence and phase contrast microscopy image showing human CD8+ T cells and MDA-MB-436 breast cancer cells (red). The red fluorescence highlights the cancer cells, while the phase contrast reveals the T cells and their interactions with the cancer cells. Alkaline comet assay revealing DNA breaks in MDA-MB-436 breast cancer cells after treatment with the DNA-damaging agent Camptothecin (CPT). The comet-like tails indicate the extent of DNA damage.
Alkaline comet assay revealing DNA breaks in MDA-MB-436 breast cancer cells after treatment with the DNA-damaging agent Camptothecin (CPT). The comet-like tails indicate the extent of DNA damage.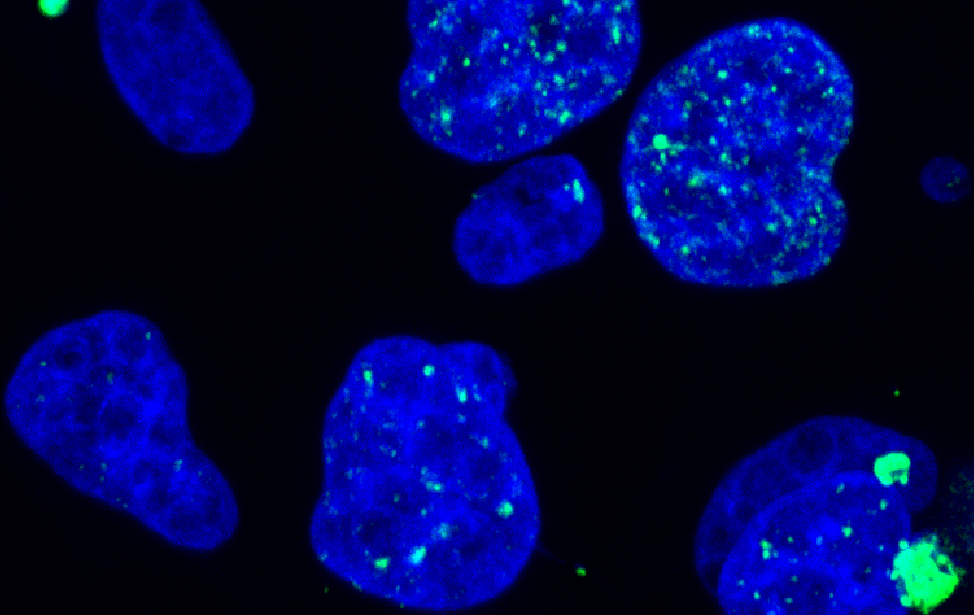 Immunofluorescence staining of MDA-MB-436 breast cancer cells showing γH2AX foci (green), marking DNA damage response activation. Nuclei are counterstained with DAPI (blue), revealing their shape and micronuclei.
Immunofluorescence staining of MDA-MB-436 breast cancer cells showing γH2AX foci (green), marking DNA damage response activation. Nuclei are counterstained with DAPI (blue), revealing their shape and micronuclei.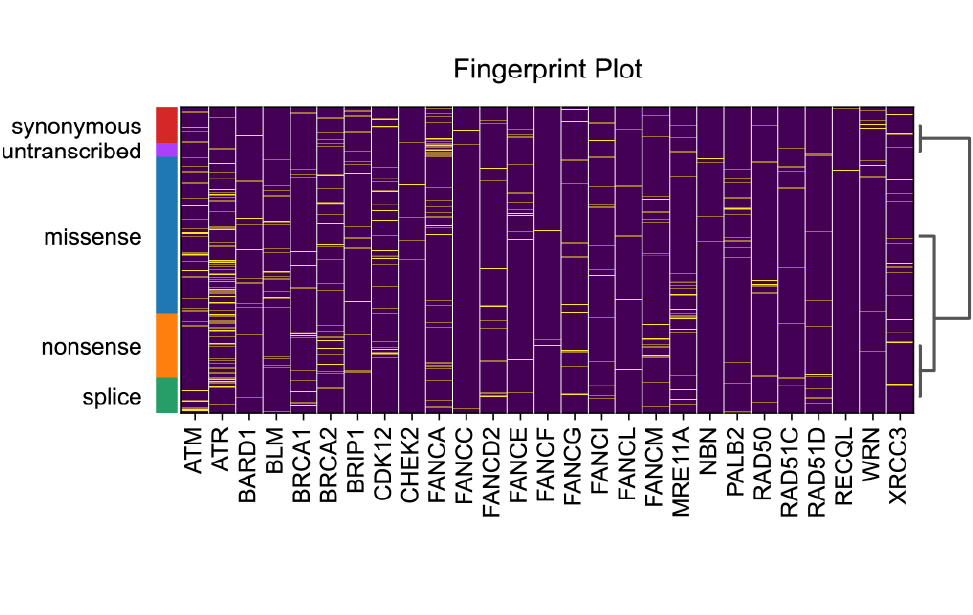 Fingerprint plot of mutation data resulting from CRISPR-mediated base editing screens in DDR (DNA damage response) genes.
Fingerprint plot of mutation data resulting from CRISPR-mediated base editing screens in DDR (DNA damage response) genes.